
Центр по изучению мелких животных, Великобритания
Основные положения
• Эпилептический статус — очень опасное заболевание. Для его успешного лечения требуется незамедлительная комплексная терапия, направленная как на купирование припадков, так и на ликвидацию системных нарушений, вызванных патологией.
• Своевременное выявление и устранение причин припадков имеет особенно важное значение при лечении эпилептического статуса.
• Наиболее распространенные лекарственные препараты, применяемые при терапии эпилептического статуса — диазепам, фенобарбитал, бромид калия, пентобарбитал и пропофол.
Введение
Эпилептический статус (ЭС) — состояние, характеризующееся частыми и длительными судорожными припадками. ЭС встречается как у собак, так и у кошек. Обычно ЭС развивается как осложнение других заболеваний. Частота наблюдений ЭС в ветеринарной медицине не фиксировалась. Однако у собак, по данным литературы, ЭС и фокальные судорожные припадки отмечаются примерно у 0,44% от общего числа больных животных, приведенных к ветврачу.
ЭС можно определить, как частые судорожные припадки, продолжающиеся свыше 30 минут (или как 2 или более следующих друг за другом припадков, в промежутках между которыми животное полностью в сознание не приходит). Животному требуется оказать помощь до истечения 30 минут с момента начала припадка. Практически все типы припадков могут стать длительными или повторяющимися (а, следовательно, требующими более тщательного лечения, чем единичный припадок).
При ЭС необходимо немедленное лечение, поскольку это состояние может привести к необратимым неврологическим нарушениям и даже к смерти пациента. Кроме того, по данным литературы при раннем агрессивном лечении затянувшегося припадка не только удается его быстрее купировать, но и применить меньшие дозировки препаратов. При такой терапии существенно возрастает и шанс па успех последующего длительного лечения. Если своевременная помощь животному во время припадка не оказана, у него развиваются глубокие нарушения гемодинамики и метаболизма, которые могут привести летальному исходу. Несвоевременное же применение противосудорожных средств может еще более углубить имеющиеся нарушения гемодинамики. Таким образом, лечение при ЭС должно быть своевременным, комплексным, осуществляться в динамике и с применением индивидуального подхода в каждом конкретном случае в зависимости от имеющейся клинической симптоматики.
Обязательный компонент терапии ЭС — быстрое прерывание припадка и стабилизация состояния животного. Быстрое распознавание и лечение факторов, провоцирующих припадки, например, менингоэнпефалита или гипогликемию, позволяет предупредить дальнейшее повреждение нейронов. Для прерывания припадка часто применяются препараты из группы бенздиазепинов, например, диазепам. Они весьма эффективны, но их действие носит кратковременный характер. Для более длительной противосудорожной терапии предпочтительнее использовать фенобарбитал. Лечение особо устойчивых припадков обычно требует комплексного применения пентобарбитала или пропофола.
В данном обзоре рассмотрены причины и последствия ЭС у домашних животных, а также способы лечения этого состояния в условиях стационара. Речь пойдет, в основном, о характерных для ЭС тонико-клонических припадках, поскольку именно они обычно наблюдаются на практике и наиболее часто приводит к смерти животного.
Патофизиология
Хотя ЭС является патологией центральной периной системы, при развитии заболевания наблюдаются глубокие патофизиологические сдвиги в функциях почти всех органных систем организма. Эти сдвиги в значительной степени и определяют гибель пациентов при ЭС. В патогенез ЭС вовлечено много различных факторов, но исход состояния определяется, в основном, постоянным системным стрессом вследствие непрекращающихся припадков и развивающихся повреждений нейронов. Взаимосвязь между этими факторами и их относительный вклад в патогенез ЭС были исследованы в моделях этого заболевания па животных. Из результатов исследований вытекает, что вероятность прерывания припадка и непрерывного повреждения нейронов определяется характером заболевания, вызвавшего ЭС, и длительностью его протекания.
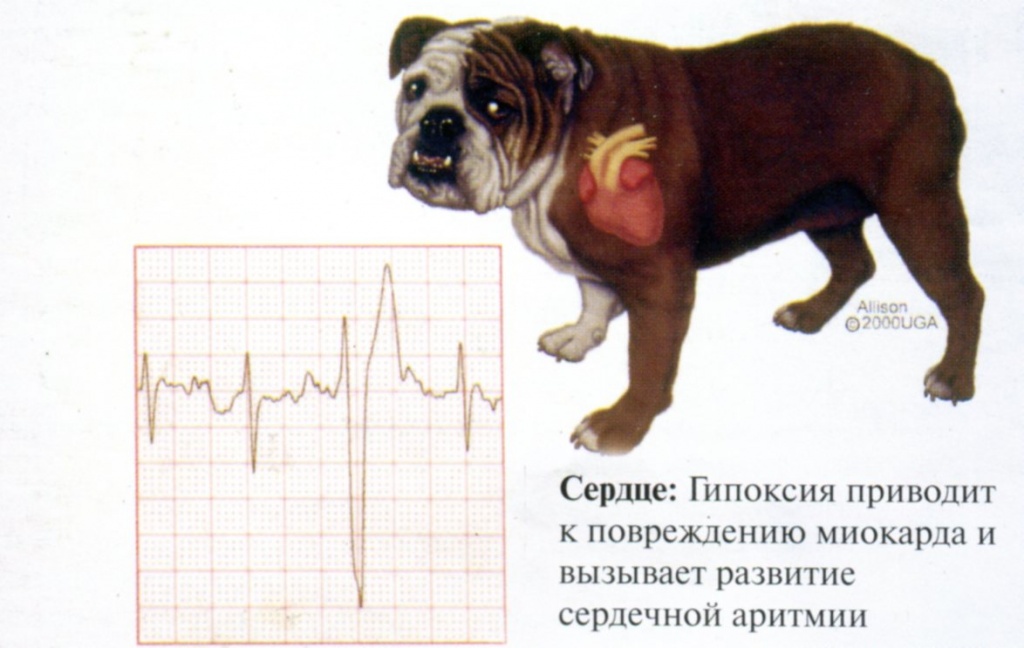
Рисунок 1. В начале припадки наблюдается нарушение сердечного ритма, проявляющееся в виде тахикардии. Однако в дальнейшем из-за гипоксии, ацидоза и угнетения функции миокарда появляется аритмия.

Рисунок 2. Из-за длительных мышечных сокращений у пациента может развиться гипертермия, приводящая к рабдомиолизу.
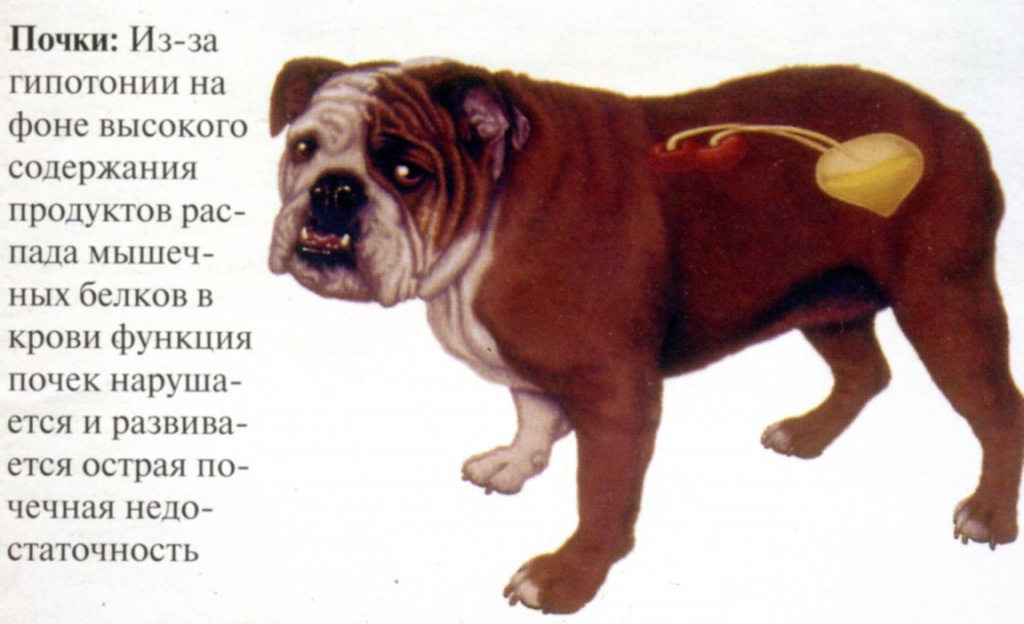
Рисунок 3. Из-за системной гипотонии и большого содержания продуктов распада мышечных белков в крови может развиться острая почечная недостаточность.
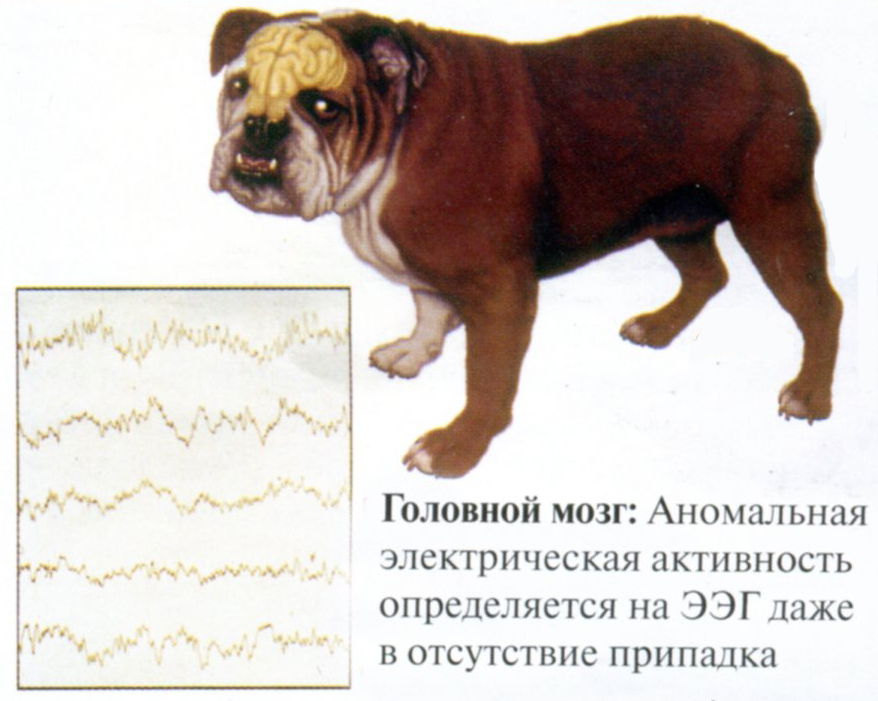
Рисунок 4. Даже в отсутствие внешних признаков припадка на ЭЭГ при эпилептическом статусе, легко заметны зоны аномальной активности коры головного мозга.
На ранних стадиях развития ЭС сопровождается нарушениями в периферической нервной системе, проявляющимися в тахикардии, гипертонии, гипергликемии (Рисунок 1). Повышение системного артериального давления приводит к существенному увеличению объема кровотока через головной мозг. Эта компенсаторная реакция направлена на удовлетворение возрастающих метаболических потребностей чрезмерно активной нервной ткани. Если припадок не прекращается, примерно через 30 минут развивается срыв адаптации и наблюдается резкое падение артериального давления. В это же время развиваются гипогликемия, гипотермия и гипоксия. Из-за срыва регуляции кровообращения кровоток через мозг становится зависимым от артериального давления, и в условиях несоответствия кровоснабжения метаболическим запросам мозга, может произойти необратимое повреждение нервной ткани. Помимо повреждения нервной ткани при длительном судорожном припадке вследствие непрерывных сокращений и нарушения дыхания развиваются метаболические отклонения в скелетной мускулатуре, приводящие к высвобождению в кровь большого количества молочной кислоты, ацидозу, гиперкалиемии, гипоксии, повышению содержания углекислоты в крови и гипертермии (Рисунок 2). Выход в кровь большою количества миоглобина и развитие миоглобинурии на фоне сниженного системного артериального давления может сильно нарушить функцию почек пациента (Рисунок 3).
Неотъемлемая часть патогенеза ЭС — нарушение механизмов, обеспечивающих самопрерывание припадка и переводящих нервную систему в рефрактерное состояние, при котором развитие новою припадка невозможно. Из-за нарушения этих механизмов при ЭС новый припадок развивается на фоне неполного восстановления функции нервной системы от повреждений, вызнанных предыдущим припадком. Показано, что многие нейроны головного мозга обладают спонтанной спайковой активностью. В отдельных группах нейронов спонтанная активность нейронов синхронизирована и ритмизирована. Припадок обычно развивается вследствие нарушения в прилегающих к данным нейронным группам нервных клетках баланса между возбуждением и торможением. По сути своей припадок — это синхронизированное возбуждение целой группы нейронов с повышенной чувствительностью к активирующим факторам (Рисунок 4) (4).
В развитии припадка принимают участие несколько нейромедиаторов. Критическим модулятором функции нейронов в головном мозге в данном случае является у-аминомасляная кислота (ГАМК). Воздействуя на постсинаптические мембраны нейронов гиппокампа, она вызывает развитие тормозных постсинаптических потенциалов, противостоящих возбуждающим импульсам, приходящим в эти нейроны из других участков мозга. В настоящее время появляется все больше доказательств того, что именно сбой ГАМК-эргической регуляции и является основной причиной возникновения припадка на молекулярном уровне. Однако при ЭС существенной частью патогенетических механизмов (как уже указывалось выше) является нарушение механизмов прерывания отдельного припадка, которое происходит либо вследствие очень сильного возбуждения, либо вследствие недостаточно эффективного торможения (3). Можно полагать, что в каждом конкретном случае ведущую роль играет свой фактор, определяемый причиной припадков. Специальные исследования показали, например, что при длительных припадках может произойти существенное нарушение функции рецепторов ГАМК на мембранах нейронов. Эти нарушения — следствие метаболических сдвигов в повторно возбуждающемся нейроне, усиливающих стимулируемое глутаматом возбуждение и блокирующих ГАМК-зависимое ингибирование. Изложенная теория получила название гипотезы повреждения нейронов вследствие токсического перевозбуждения (4). При больших концентрациях кальция в среде его ионы могут проникать в цитоплазму нейронов. Повышение концентрации ионов кальция в цитоплазме запускает целый каскад внутриклеточных нейрохимических механизмов, приводящих клетку к гибели. К нейротоксичпым соединениям, высвобождающимся при ЭС. относятся аспартат. свободные жирные кислоты, арахидоновая кислота, а также свободные радикалы.
Этиология и исход ЭС
В последнем исследовании показано, что при обращении в ветклинику владельцев собак по поводу эпилептических припадков у их питомцев, первичную причину заболевания не удается установить примерно в 25,8% случаев (6) (Таблица 1). Приблизительно 27% случаев заболевания классифицируются как первичная эпилепсия наследственного или идиопатического характера. У 35% животных эпилептические припадки являются вторичным проявлением другого заболевания — эпилепсия у них приобретенная, вторичная. В 7% случаев наблюдаются реактивные эпилептические припадки (6). При реактивной эпилепсии значимых нарушений в структуре головного мозга не выявляется, а причиной припадков являются интоксикация, системные, метаболические или гормональные заболевания (7). Одним из хронических заболеваний, при которых может развиться ЭС. является эпилепсия. При ее наличии ЭС может развиться как при попытке прервать припадок, так и при внезапном прекращении приема противосудорожных препаратов. В ходе вышеупомянутого исследования у 6% собак с ЭС в крови была выявлена аномально низкая концентрация таких препаратов, что и явилось непосредственной причиной развития ЭС. Автор публикации недавно завершил обследование, проводившееся на группе из 50 собак с генерализованной конвульсивной формой ЭС (8). У 28% этих животных в анамнезе была первичная эпилепсия, у 32% — эпилепсия носила вторичный характер, а у 12% — эпилепсия была реактивной. В 28% случаев причину развития ЭС выявить не удалось. У 36% собак с ЭС (12 из 33), наблюдались отклонения в составе спинномозговой жидкости (СМЖ). В группе собак с фокальными припадками такие отклонения наблюдались в 73,5% случаев (у 75 животных из 120 обследованных).
Данных по смертности собак с ЭС пет. Это в большой степени связано с тем. что многие владельцы больных животных предпочитают усыплять своих питомцев. У людей, по данным литературы, смертность от ЭС варьирует от 3 до 22%. Одна из причин — смертность собственно от ЭС в ветеринарной медицине не установлена — сложность интерпретации причины гибели животного при наличии у него многих заболеваний, которые могут привести к развитию ЭС. Поданным автора у 46% животных с ЭС при проведении магнитно-резонансного обследования или рентгеновской компьютерной томографии выявляются отклонения в структуре головного мозга.
Устранение причин ЭС
Во многих случаях ЭС развивается у животных, ранее страдавших хроническими эпилептическими припадками. К сожалению, точной оценки частоты таких случаев в ветеринарной медицине нет. Другие заболевания, приводящие к развитию ЭС — это опухоли, системные инфекционные поражения центральной нервной системы, травмы, метаболические отклонения (например, электролитный дисбаланс) и нарушения кровообращения.
С учетом вышеизложенного при первичном осмотре пациента с ЭС прежде всего нужно обследовать его череп и позвоночник на предмет наличия недавних травм. Голову и позвоночник следует аккуратно пальпировать. Признаками травмы являются крепитация, болезненность, асимметрия. При лабораторном тестировании, кроме обычных показателей, следует определить содержание в крови глюкозы, натрия. кальция, а также активности ферментов печени и показатели функции почек. Необходимо также определить активность ацетилхолинэстеразы в сыворотке крови. Нужно отметить, что в течение некоторого времени сразу после припадка из-за гипоксии и гипотензии активность ферментов печени в крови у животного может быть повышена. Если есть основания предполагать, что причиной ЭС является гипогликемия (или если нет возможности определить концентрацию глюкозы в крови животного), следует ввести пациенту внутривенно в течение 15 минут 50% раствор глюкозы (желательно предварительно разбавить его до 25%) в дозе 0.5 г/кг веса (8). Если установлено, что до развития ЭС животному давали фенобарбитал или другие противосудорожные препараты, желательно определить концентрацию этих препаратов у него в крови. При подозрении на энцефалит нужно сделать анализ спинномозговой жидкости (СМЖ) сразу же после выведения пациента из припадка и стабилизации его состояния. Применение глюкокортикоидов позволяет предупредить развитие отека мозга и воспаления, вызванных гипоксией. Однако кортикостероиды, действуя на нейроны непосредственно во время ишемии, усиливают гипоксическое повреждение нервной ткани и угнетают ее репарацию после устранения гипоксии. При ЭС глюкокортикоиды нужно применять только после прерывания припадка и только для предупреждения распития отека мозга при признаках увеличения внутричерепного давления у животного. Действие больших доз метилпреднизолона при ЭС не исследовалось, но на экспериментальных моделях было показано, что применение этого гормона сразу после повреждения головного мозга, сопровождающегося отеком, существенно улучшает исход заболевания и снижает смертность.
| Классификация и причины развития эпилептического статуса |
| Первичная эпилепсия |
| Идиопатическая Породная предрасположенностьНаследственная |
| Вторичная эпилепсия |
| Менингоэнцефалиты— инфекционные
Вирусные риккетсиозные простейшими грибковые бактериальные — стерильные грануломатозные энцефалиты Новообразования — первичные (опухоли нервной системы) менингиома астроцитома олигодендроглиома папиллома паутинной оболочки — вторичные лимфома |
| Реактивная эпилепсия |
| Нарушения метаболизма
— почечная/ гепатогенная/ диабетическая энцефалопатия — нарушение ионного баланса — гипогликемия Интоксикации |
| Другие причины эпилепсии |
| Нарушение режима приема противосудорожных препаратов и резкое снижение их концентрации в крови |
Животным с внезапно начавшимися припадками следует назначить обследование мозга методами ЯМТ- или рентгеновской компьютерной томографии. Однако лаже если эти методы ничего не выявляют, полностью исключить патологию мозга нельзя.
В целом, терапия при ЭС приносит успех при комплексном подходе, включающем в себя меры по стабилизации состояния животного и по его интенсивному лечению, а также диагностические мероприятия, проводимые одновременно. В это же время следует подробно опросить владельца животного для выяснения всех особенностей развития болезни у его питомца. Полезно также ознакомиться со всеми данными анамнеза.
Значение электроэнцефалографии
Хотя первичный диагноз ЭС может быть поставлен на основании имеющейся клинической симптоматики, дальнейшая диагностика и лечение патологии будет осложнена, если не провести электроэпцефалографического обследования (ЭЭГ). Поскольку из исследований на моделях ясно, что пароксизмальная активность мозга может вызвать его повреждение даже в отсутствие генерализованного припадка, именно эту активность и следует стремиться устранить в ходе лечения пациента с ЭС (Рисунок 4). Начальные формы пароксизмальной активности на ЭЭГ проявляются в виде дискретных аномальных волн и ритмических спаек, которые отличаются необычно большой продолжительностью. В дальнейшем эти волны и спайки объединяются в спайково-волновые группы, появляются ритмические широкие и медленные волны, прерываемые периодами относительного спокойствия, которые становятся все более продолжительными по мере сокращения периодов повышенной активности. Эти периоды электрического молчания мозга указывают на переход пациента с ЭС в коматозное состояние, даже если у него и наблюдаются слабые конвульсивные движения. К сожалению, подробных обследований ЭЭГ животных с ЭС в ветеринарной практике не проводилось. В идеале же этот метод должен быть наиболее информативен при оценке состояния пациентов, пребывающих в коме, а также при оценке эффективности терапии ЭС тем или иным препаратом, если результат не очевиден. Если же принятые меры привели к исчезновению клинических признаков припадка и к пациенту возвращается сознание, регистрацию ЭЭГ можно и не проводить. При терапии ЭС, в отличие от многих других случаев, нельзя прерывать лечение в ожидании прибытия энцефалографа и получения ЭЭГ. Однако после купирования припадка этот метод может быть чрезвычайно полезен для выяснения причин развития ЭС у кошек и собак.
Системная стабилизация животных с ЭС
Прежде всего, к животным с ЭС необходимо применить весь комплекс мер неотложной помощи, направленных на спасение их жизни.
Оксигенация, восстановление проходимости дыхательных путей, коррекция кислотно-основного баланса
Восстановление проходимости дыхательных путей и нормализация дыхания у животных с ЭС — задача непростая. Лучше всего провести мероприятия по восстановлению функции дыхательных путей во время их пребывания в бессознательном состоянии. Животным рекомендуется вводить чистый кислород, либо с помощью дыхательной маски, либо через носовые зонды.
У животных с ЭС весьма эффективным оказывается мониторинг газов артериальной крови (ГАК). Это связано с тем, что вследствие интенсивных и длительных конвульсий у них часто развивается метаболический ацидоз. При выявлении с помощью анализа ГАК гипоксии или респираторного ацидоза пациента следует лечить немедленно. Метаболический ацидоз обычно проходит самопроизвольно после прерывания судорожного припадка.
Установка внутривенных катетеров
Для введения жидкости и лекарственных препаратов пациенту с ЭС следует установить большой внутривенный катетер. Через катетер вводится физиологический раствор с добавкой хлористого калия. Скорость введения должна быть постоянной. С помощью жидкостной терапии можно устранить возникающие у больного животного нарушения электролитного баланса.
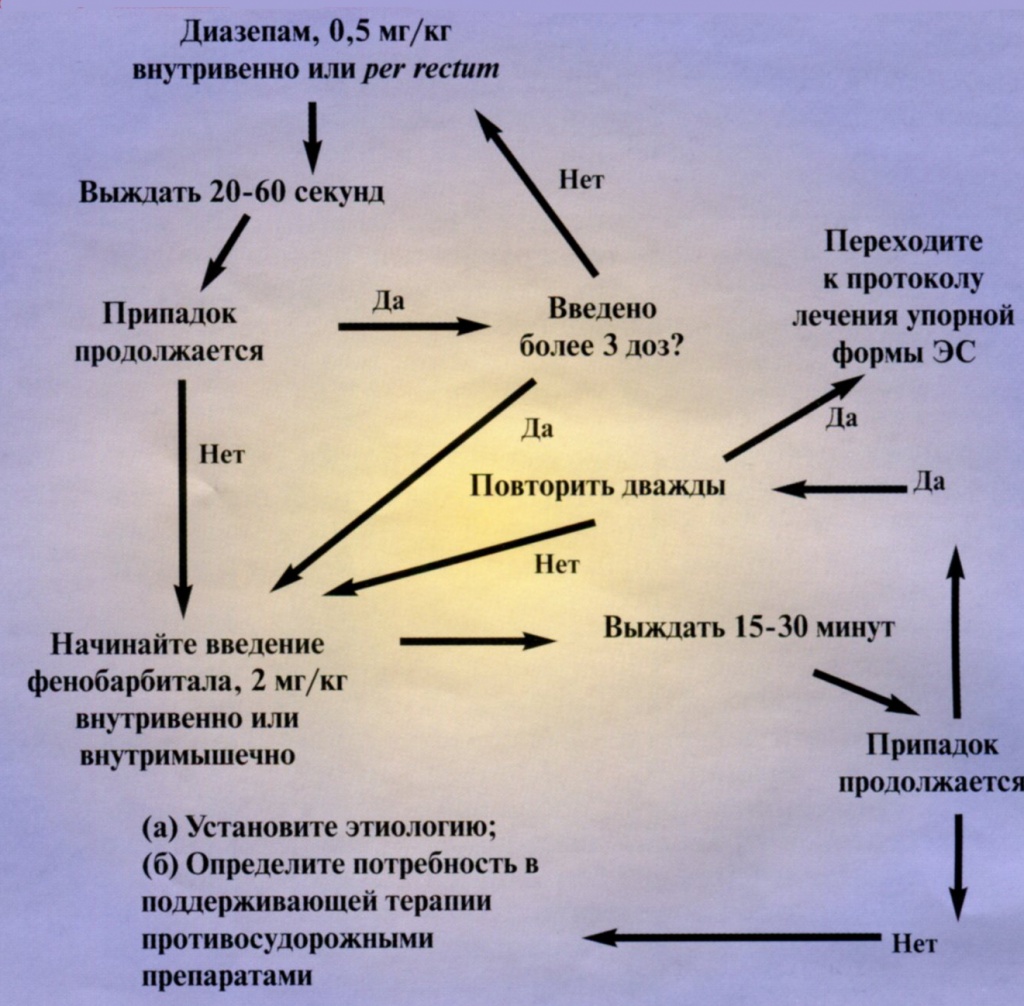
Рисунок 5. Протокол лечения эпилептического статуса в ветеринарной медицине.

Рисунок 6. Протокол лечения устойчивого эпилептического статуса в ветеринарной медицине.
Регуляция температуры тела
Развивающаяся при ЭС гипертермия вызывает ускоренный распад белков в скелетных мышцах. Продукты распада, появляющиеся в больших количествах в крови пациента, могут привести к развитию острой почечной недостаточности. Для предупреждения этого осложнении в ходе терапии ЭС показано применение мер по регуляции температуры тела пациента. Эти меры особенно необходимы, если температура тела пациента поднимается свыше 40° С. При охлаждении тела больного животного для предупреждения гипотермии следует следить за ректальной температурой. Процесс охлаждение тела нужно прерывать, если температура тела опустилась ниже 40° С.
Первоначальная медикаментозная терапия ЭС
В настоящее время стандартных рекомендаций по медикаментозной терапии ЭС в ветеринарной медицине не существует. Для лечения патологии применяют разные методы в зависимости от индивидуальных особенностей животного.
Известно, что препараты бензодиазепинового ряда (диазепам, лоразепам. мидазолам и клоназепам) являются чрезвычайно мощными противосудорожными средствами (особенно диазепам), поэтому эти лекарственные средства применяются для первоначальной терапии ЭС (5). Действие этих препаратов опосредуется стимуляцией пре- и постсинаптических ГАМК-эргических рецепторов через бензодиазепиновые рецепторы. Однако для длительного лечения ЭС бензодиазспины не подходят, так как, в основном, это препараты седативного и транквилизирующего действия с разной продолжительностью действия и разной эффективностью. К побочным эффектам бензодиазепинов относятся угнетение дыхания, гипотензия и нарушение сознания. К несчастью, дозу диазепама. которая может вызвать остановку дыхания у животного, определить трудно.
В ветеринарной медицине при лечении ЭС наиболее часто применяется диазепам. Из-за кратковременного действия этот препарат не подходит для длительной терапии. При внутривенном введении, однако, в течение некоторого непродолжительного времени в крови и в тканях головного мозга концентрация препарата остается достаточно высокой, в результате чет диазепам считается эффективным средством терапии ЭС. Поскольку при ЭС припадок может прерваться спонтанно, не следует вводить диазепам пациентам без судорожных проявлений, за исключением тех случаев, когда у них на лицо явные признаки приближающегося повторного припадка. Рекомендуемая дозировка диазепама и у собак, и у кошек — 0,5-1 мг/кг. Препарат вводится внутривенно или ректально. Общая доза лекарственного средства, вводимая пациенту во время начальной стадии терапии ЭС, не должна превышать 20 мг (10). Повторить введение диазепама животному можно не ранее, чем через 2 часа после применения максимальной дозировки (Рисунок 5). Благотворно действует на животное также непрерывное внутривенное введение диазепама (9). Скорость введения препарата (в виде раствора в 5% водном растворе глюкозы) должна составлять 2-5 м г/час. Если с помощью диазепама не удается прервать припадок, следует ввести животному фенобарбитал.
Наиболее частая и наиболее опасная для жизни животного ошибка, которую допускают ветеринарные врачи при терапии ЭС. — купирование повторных припадков возрастающими дозами диазепама без применения противосудорожных препаратов пролонгированного действия. В таких случаях купировать повторные припадки, как правило, не удается, зато в крови пациента накапливаются токсические количества диазепама и его метаболитов. Именно передозировка диазепама может привести пациента к смерти.
В некоторых случаях ввести животному внутривенно диазепам невозможно. Таким пациентам лекарственные препараты вводят внутримышечно, хотя при этом сложно предсказать скорость и эффективность всасывания лекарственного средства в кровь. Можно применять диазепам и per rectum. Начальная доза препарата при таком применении от 0,5 до 2 мг/кг, в зависимости от того, применялся ли у данного пациента фенобарбитал для купирования первичного припадка. Если пациент в течение длительного времени получал фенобарбитал в качестве основного противоэпилеитпческого препарата, дозировку диазепама нужно увеличить. У собак, не получавших противоэпилептических средств, при применении препарата per rectum в дозе 1 мг/кг концентрация диазепама в крови достигает терапевтических значений через 14.3 минуты. Максимальная концентрация, которую можно достичь в таких случаях, составляет 474 мг/л. что существенно выше, чем нужно для оказания противосудорожного действия (300 мг/л).
Фенобарбитал
Фенобарбитал — относительно безопасное средство, которое можно применять per os, внутривенно и внутримышечно. Фенобарбитал повышает порог возбудимости нервной ткани и снижается риск развития припадка. Кроме того, фенобарбитал предупреждает распространение пароксизмальной электрической активности из очагов возбуждения на окружающие их нейроны. На молекулярном уровне причиной такого действия фенобарбитала является активация в его присутствии ГAMK-эргических рецепторов постсинаптических мембран и усиление тормозящего эффекта ЕАМК. Фармакологическое действие фенобарбитала начинается через 30 мин. после его введения, что связано с меньшей по сравнению с диазепамом липофильностью этого препарата. Этот факт необходимо принимать во внимание при использовании фенобарбитала для купирования судорожного припадка. Рекомендуемые дозы фенобарбитала — 12-24 мг/кг внутривенно, если требуется максимально ускорить ею терапевтическое действие. Если быстрый эффект не требуется, начальная доза препарата может быть 2 мг/кг внутривенно с повторным се введением каждые 20-30 минут вплоть до проявления действия. Максимальная суточная доза фенобарбитала не должна превышать 24 мг/кг (Рисунок 5). Возможно и внутримышечное введение фенобарбитала. Такой способ введения данного препарата чаше всего применяется на фоне предварительного внутривенного введения пациенту диазепама, поскольку в таком режиме фенобарбитал не потенцирует угнетающее действие диазепама на дыхание и кровообращение. Побочные эффекты фенобарбитала (угнетающее действия на дыхательную и кровеносную системы, помутнение сознания) иногда существенно затрудняют его применение при ЭС, особенно при использовании в комплексе с бензодиазепинами. Поэтому перед применением фенобарбитала следует интубировать пациента и быть готовым применить искусственную вентиляцию легких.
Бромистый калий
Бромистый калий (КВr) — весьма распространенное поддерживающее противосудорожное средство у кошек и собак. Время полувыведения КВr из организма собаки при однократном применении этого препарата per as составляет 25 дней, что исключает его использование для терапии ЭС. В последнем исследовании было показано, что КВг прекрасно всасывается и при введении per rectum. При таком введении усваивается примерно 57,7% введенной дозы КВт, а среднее время полувыведепия препарата составляет 20,4 дня (12). Вводить препарат per rectum удобно животным, которые находятся в бессознательном состоянии после применения фенобарбитала и/или диазепама. Насыщающая доза КВг (600 мг/кг) может быть введена per os в течение 24 часов, либо per rectum (100 мг/кг за одно введение, повторять каждые 4 часа). Побочное действие при применении КВг — диарея и сильный седативный эффект.
Лечение
Если связанный с ЭС припадок не удается купировать с помощью фенобарбитала или бенздиазепинов, у пациента протекает упорная форма ЭС, требующая более агрессивной терапии (Рисунок 6). Причинами устойчивости ЭС к медикаментозной терапии могут быть неправильно подобранные лозы противосудорожных препаратов, не полностью устраненные метаболические нарушения и наличие внутричерепной патологии (например, новообразования). Таких животных очень трудно лечить. В случаях упорного ЭС применяют анестетики короткою действия. Их эффект наступает быстро, время пребывания в организме пациента невелико, а скорость метаболических процессов в нервной ткани после их применения значительно снижается. Однако применять эти препараты нужно только в условиях палаты интенсивной терапии, поскольку при их использовании необходим постоянный мониторинг артериального давления или (что еще лучше) давления крови в венах головного мозга. Введение пациента в состояние обшей анестезии предупреждает тонико-клонические судороги и позволяет контролировать состояние ею дыхания.
Пропофол
В медицине внутривенное введение анестезирующих доз пропофола (2,6-диизопропилфенола) — стандартный метод лечения устойчивых форм ЭС (13). Однако в ветеринарной медицине этот метод практически не применяется. Пропофол обладает одновременно барбитурат- и бенздиазепиноподобным действием и может в значительной степени снизить скорость метаболизма в центральной нервной системе. Применять пропофол можно как путем однократной внутривенной инъекции, так и путем непрерывного введения через внутривенный катетер с постоянной скоростью (0,1-0,6 мг/кг/минуту) (14). Применение данного препарата требует осторожности, желательно, чтобы пациент находился в специально оборудованной палате интенсивной терапии, где имеются условия для перехода на искусственное дыхание и возможна поддержка системы кровообращения. Частым побочным эффектом пропофола является апноэ (остановка дыхания) и развивающаяся на его фоне гипоксемия с угнетением работы сердца.
Барбитураты
Очень эффективны при упорных формах ЭС тиопентал и пентобарбитал. При правильно подобранных дозировках эти барбитураты почти всегда снимают внешние проявления припадка. Однако вызываемое ими резкое снижение артериального давления ограничивает их применение. Пентобарбитал (натриевая соль) при применении в стандартных дозах — общий анестетик с выраженным прогивосудорожным действием. Тиопентал чаще, чем пентобарбитал, оказывает токсическое действие на миокард. В одном исследовании при введении собакам больших доз тиопентала, необходимых для угнетения пароксиз-мальной активности на ЭЭГ, из 7 животных погибло 5. В аналогичных условиях введение пентобарбитала не вызывало гибели собак (выжили все 17 экспериментальных животных). Дозировка пентобарбитала подбирается строго индивидуально, по эффекту, и часто не совпадает с рекомендуемой (3-15 мг/кг внутривенно) (Рисунок 6) (15). При лечении ЭС с помощью «барбитуратной комы» часто требуется длительное искусственное дыхание. Побочные эффекты «барбитуратной комы» — угнетение метаболизма в миокарде, вазодилятация с венозным застоем и ухудшение кровоснабжения сердца. Ослабить эти побочные эффекты можно за счет введения пациенту физиологического раствора и небольших доз дофамина. Из-за гипотензии и угнетения функции сердца у пациентов может развиться пойкилотермия и анурия. В состоянии «барбитуратной комы» практически невозможно провести неврологическое обследование пациента, поскольку у него отсутствуют дыхательные движения и мышечная активность. Единственный метод наблюдения за состоянием центральной нервной системы в таких случаях — регистрация ЭЭГ. В клинике автора статьи «барбитуратная кома» применяется только в те случаях, когда попытки купировать припадок с помощью диазепама и/или фенобаритала не дали результата.
Ингаляционная анестезия
В особо устойчивых случаях ЭС можно рекомендовать ингаляционную анестезию. К сожалению, в условиях ветеринарной клиники не всегда имеется необходимое для ее проведения оборудование и обученный соответствующим образом персонал. Чаще всего для лечения ЭС применяют ингаляционный анестетик изофлуран. Нужно иметь в виду, что не нее ингаляционные анестетики обладают противоэпилептическим действием. Энфлуран, например, может даже стимулировать судорожный припадок. Что касается изофлурана, то это соединение не метаболизируется печенью, даст быстрый эффект и в настоящее время интенсивно исследуется как противосудорожное средство. Конечно, применение изофлурана требует искусственною дыхания и может осуществляться только в условиях операционных или палат интенсивной терапии. Возможное осложнение при применении изофлурана — резкая гипотензия.
Заключение
Основная цель при лечении пациентов с ЭС — быстрое купирование судорожного припадка. Достижение этой цели требует от ветеринарного врача определенных знаний, в частности, понимания механизма действия противосудорожных препаратов. На основании этой информации разрабатывается план последовательного использования противосудорожных средств, применяемых в ветеринарной медицине. Неправильное использование противосудорожных препаратов у пациента с выраженным нарушением функции мозга может не только сильно осложнить дальнейшее лечение, но и стать для него фатальным. Даже при правильном использовании противоэпилептических препаратов в палатах интенсивной терапии часто наблюдаются побочные эффекты в виде нарушения дыхания и кровообращения. Это требует непрерывного мониторинга показателей функции дыхания и кровообращения во время терапии ЭС. Успех лечения ЭС возможен только при комплексном подходе к терапии.
